- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
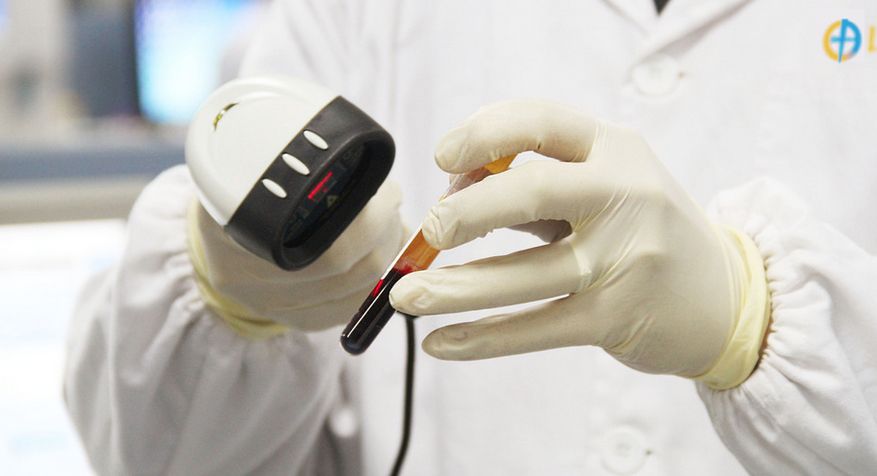
醫療器械臨床數據統計分析 醫療器械臨床試驗是初步的臨床人體安全、有效性的評價試驗。隨著科技的飛速發展,醫療器械的研發逐年增多,提高醫療器械臨床研究水平顯得更加重要。醫療器械的門類、功效非常多,為應對特定醫療器械的功效,應根據產品特點進行相應的科學設計,統計分析方法需結合研究設計類型和資料特征進行選擇。 時間:2019-6-24 0:00:00 瀏覽量:3069
-
醫療器械臨床試驗的倫理審查:招募受試者 招募合格的受試者在醫療器械臨床試驗過程中是至關重要的,而且可能是最困難、最富有挑戰性的工作。受試者招募的倫理審查主要包括招募的方式,受試人群的選擇與激勵補償措施。招募方式必須考慮尊重隱私與自愿參加的原則,避免強迫和不正當影響。受試人群的選擇必須考慮受益和負擔公平分擔和試驗人群的代表性問題。對受試者參加試驗的激勵補償必須考慮合理補償與避免過度勸誘的問題。 時間:2019-6-22 22:19:37 瀏覽量:4358

-
關于醫療器械臨床試驗用注冊檢驗報告一年有效期問題 早在2017年7月31日,總局就對醫療器械臨床試驗用注冊檢驗報告一年有效期和臨床試驗備案問題做了解讀。對注冊檢驗報告一年有效期作出了明確的規定,相對之前,時間有所放寬,企業又更多的時間準備。 時間:2019-6-21 0:00:00 瀏覽量:9727

-
二類醫療器械臨床試驗存在的主要問題 自2016年7月26號山東省食品藥品監督管理局發布《山東省食品藥品監督管理局關于開展醫療器械臨床試驗監督抽查工作的通告》以來,山東省對二類醫療器械臨床試驗展開監督抽查,發現存在臨床試驗數據存在不真實、不完整、無法溯源,臨床試驗質量低劣、相關記錄缺失等一系列問題。 時間:2019-6-20 22:39:30 瀏覽量:3431

-
臨床試驗機構方面在醫療器械臨床試驗中存在的問題與建議 通過對申辦方二類醫療器械臨床試驗的監督抽查,發現存在臨床試驗過程不規范、個別真實性和一系列規范性問題,需要臨床試驗機構和研究者形成統一共識,重視臨床試驗的發展,重視法律法規的規范執行,保證臨床試驗用樣本真實性、有效性。 時間:2019-6-19 0:00:00 瀏覽量:2411

-
最新!醫療器械臨床試驗機構備案達770家 近日在醫療器械臨床試驗機構備案系統中獲悉,截止目前,已有770家醫療器械臨床試驗機構。其中,603家也是藥物臨床試驗資格認定機構。 時間:2019-6-18 0:00:00 瀏覽量:2569

-
醫療器械臨床試驗的前提條件 醫療器械臨床試驗,是指在經資質認定的醫療器械臨床試驗機構中,對擬申請注冊的醫療器械在正常使用條件下的安全性和有效性進行確認或者驗證的過程。 時間:2019-6-17 22:54:46 瀏覽量:3481

-
第三類醫療器械臨床試驗過程 醫療器械的臨床試驗是對申辦方申請注冊的醫療器械的臨床試用或驗證的過程。《醫療器械監督管理條例》(國務院令第650號)第十九條:第三類醫療器械進行臨床試驗對人體具有較高風險的,應當經國務院食品藥品監督管理部門批準。? 時間:2019-6-16 22:27:10 瀏覽量:12004

-
醫療器械臨床試驗方案對比及樣機準備數量說明 根據《醫療器械臨床試驗質量管理規范》要求,企業產品注冊前開展的臨床試驗工作可以采用以下三種臨床試驗統計方案:單組目標值臨床試驗方案;金標準目標值臨床試驗方案;非劣效性同品種臨床試驗對比方案。 時間:2019-6-15 23:50:19 瀏覽量:3089

-
藥物、醫療器械臨床試驗有什么不同 藥物臨床試驗是適用于藥物的,參照的是《藥物臨床試驗質量管理規范》于2003年6月4日經國家食品藥品監督管理局局務會審議通過,現予發布。本規范自2003年9月1日起施行。醫療器械臨床試驗是適用于醫療器械的,參照的是《醫療器械臨床試驗質量管理規范》已經國家食品藥品監督管理總局局務會議、國家衛生和計劃生育委員會委主任會議審議通過,現予公布,自2016年6月1日起施行。 時間:2019-6-15 0:11:49 瀏覽量:4675

-
第三類高風險醫療器械臨床試驗審批服務指南 我國醫療器械法規體系的構建始于2000年《醫療器械管理條例》的實施,經過2014年、2017年的2次修訂后,法規體系的框架已經基本確立。國家對于醫療器械有著嚴格的分類,其中最高級別的第三類高風險醫療器械對人體具有較大的潛在危險,必須對其進行嚴格的準入控制,因此臨床試驗審批也是較為嚴格 時間:2019-6-13 23:05:11 瀏覽量:2863

-
總局加入ICH后的醫療器械臨床試驗要求 2017年,國家食品藥品監督總局正式加入ICH,成為其全球第8個監管機構成員。中國加入ICH,長期來看對于整個醫療器械臨床試驗行業來說,無疑是一次提升,進一步融入國際市場的契機。中國加入ICH但短期來看意味著各類標準提升,本土大部分企業可能面臨體系提升帶來的陣痛,甚至會遭淘汰。 時間:2019-6-12 23:38:58 瀏覽量:4856

-
外周藥物涂層球囊導管醫療器械臨床試驗的主要研究終點應如何選擇 周圍動脈疾病已成為威脅人類健康的全球性問題之一。隨著人口老齡化及飲食結構改變,其發生率與日俱增。據估計,目前全球有2億多的周圍動脈疾病患病人群。盡管絕大部分患者是無癥狀的,但該病的演進會直接造成跛行、靜息痛,甚至截肢,嚴重影響患者的生活質量。 時間:2019-6-11 21:41:39 瀏覽量:2641

-
如何做一名高效能的醫療器械臨床試驗的CRC? CRC是一個很有前途的職業,尤其是在研究者很忙的中國醫院中。CRC的工作職責,簡單理解是非醫學判斷類的、被PI授權的、經過培訓的臨床試驗輔助工作。“加快入組速度,提升試驗質量”是每一個醫療器械臨床試驗項目的宗旨。 時間:2019-6-10 0:00:00 瀏覽量:5363

-
醫療器械臨床試驗方案有哪些內容? 在中華人民共和國境內開展醫療器械臨床試驗,應當遵循《醫療器械臨床試驗質量管理規范》。本規范涵蓋醫療器械臨床試驗全過程,包括臨床試驗的方案設計、實施、監查、核查、檢查,以及數據的采集、記錄,分析總結和報告等。 時間:2019-6-9 23:31:59 瀏覽量:4431

-
醫療器械臨床試驗解析 隨著新版《醫療器械臨床質量管理規范》的實施,越來越多的醫療器械企業同仁在解讀規范和實踐操作中遇到了很多的困惑。 時間:2019-6-8 0:00:00 瀏覽量:5186

-
醫療器械臨床試驗機構的篩選 - 體外診斷試劑 國家局于2014年9月11日發布了《體外診斷試劑臨床試驗技術指導原則》,同時,原國家食品藥品監督管理局發布的《體外診斷試劑臨床研究技術指導原則》(國食藥監械〔2007〕240號)廢止。 時間:2019-6-6 0:00:00 瀏覽量:2548

-
浙江省人民醫院院通過浙江省醫療器械臨床試驗審批中心現場檢查 5月29日,浙江省醫療器械審評中心六位專家蒞臨浙江省人民醫院,對泌尿外科、檢驗科和消化內科三個在研的醫療器械臨床試驗進行了現場檢查。 時間:2019-6-5 21:51:32 瀏覽量:3149

-
淺談醫療器械臨床試驗知情同意:每個受試者最基本的權利 在醫療器械臨床試驗領域,作為一種特殊的醫療行為,法律為保護患者的人格權,設立了知情同意制度。 時間:2019-6-4 0:00:00 瀏覽量:4320

-
醫療器械臨床試驗審批申報資料清單及要求 第三類醫療器械進行臨床試驗對人體具有較高風險的,應當經國家食品藥品監督管理總局批準。需進行臨床試驗審批的第三類醫療器械目錄由國家食品藥品監督管理總局制定、調整并公布。 時間:2019-6-3 0:00:00 瀏覽量:4940

