- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
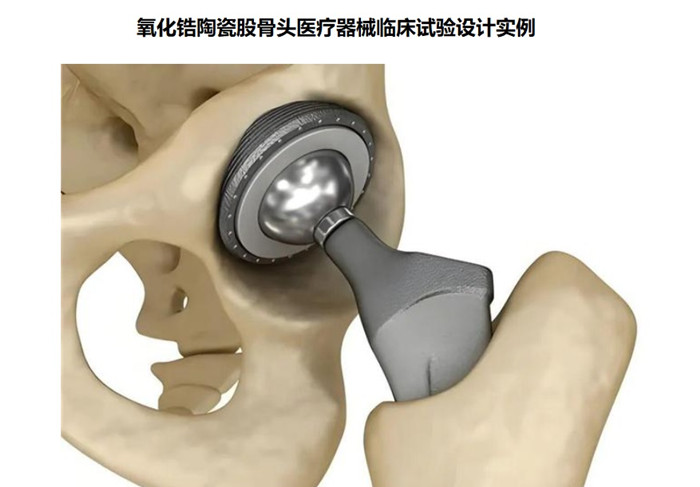
氧化鋯陶瓷股骨頭醫療器械臨床試驗設計實例 氧化鋯陶瓷股骨頭為髖關節假體組件,股骨柄部插入股骨髓腔內后, 陶瓷股骨頭與髖臼內襯、髖臼(外)杯形成旋轉關節面, 實現髖關節的運動。利用機械原理形成新的關節活動。氧化鋯陶瓷股骨頭在我國屬于第三類醫療器械注冊產品,目前,需要通過醫療器械臨床試驗完成臨床評價,本文為大家介紹氧化鋯陶瓷股骨頭醫療器械臨床試驗設計實例,一起看正文。 時間:2024-11-26 0:00:00 瀏覽量:205
-
建議新增和修訂的免于臨床試驗體外診斷試劑目錄(2024年征求意見稿) 2024年11月5日,國家藥監局發布《關于公開征求對免于臨床試驗體外診斷試劑目錄的通知》,一起來看具體內容。 時間:2024-11-5 20:15:53 瀏覽量:335
-
創新醫療器械注冊在臨床評價部分是否可以遞交同品種臨床評價報告? 關于創新醫療器械注冊產品,多數情況下,因為其具有的創新性導致在市面上很難有同類產品,而面臨醫療器械臨床試驗要求,但這并不是必然。本文為大家說說創新醫療器械注冊時在臨床評價部分是否可以遞交同品種臨床評價報告這個話題,一起看正文。 時間:2024-10-30 20:56:39 瀏覽量:276

-
呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)臨床試驗設計實例 呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)在我國屬于第三類體外診斷試劑產品,產品用于定性檢測人咽拭子樣本中的呼吸道病原體,包括甲型流 感病毒、乙型流感病毒(Victoria 系和 Yamagata 系)、腺病毒(B 組、 C 組、E 組)、呼吸道合胞病毒(A 亞型和 B 亞型)、肺炎支原體和百日咳鮑特菌。 時間:2024-10-5 22:24:12 瀏覽量:390

-
國家藥監局發布無源植入器械等六大類醫療器械臨床試驗設計類型推薦意見 2024年9月27日,在《醫療器械臨床評價推薦路徑》的基礎上,在無源植入器械、神經和心血管手術器械、口腔科器械、放射治療器械、醫用成像器械、醫用診察和監護器械等推薦開展臨床試驗的產品中,器審中心選取了典型產品, 按照產品名稱、結構組成和適用范圍,以舉例的方式給出具體產品臨床試驗設計類型(“隨機對照設計”或“可考慮采用單組設計”)的推薦意見。 時間:2024-9-27 0:00:00 瀏覽量:674

-
外科用封合劑臨床前研究及臨床試驗設計要點 外科用封合劑注冊產品在我國屬于第三類醫療器械注冊產品,且不在免于醫療器械臨床試驗醫療器械目錄內,因此,醫療器械注冊人需要通過醫療器械臨床試驗或是同品種臨床評價完成臨床評價,本文為大家說說外科用封合劑臨床前研究及臨床試驗設計要點。 時間:2024-9-26 19:44:28 瀏覽量:489

-
2024年上海市醫療器械臨床試驗機構備案后檢查情況 ?2024年3月至8月,上海市藥品監督管理局組織開展2024年上海市醫療器械臨床試驗機構備案后監督檢查和臨床試驗項目監督抽查。本次臨床試驗機構檢查內容包括機構部分和專業部分共16個環節96個檢查項目,共出動188人次,覆蓋全市43家臨床試驗機構,檢查結果為16家符合要求,27家整改后符合要求。臨床試驗項目共抽查5個,檢查內容共6個環節72個檢查項目。 時間:2024-9-24 0:00:00 瀏覽量:376

-
可以使用醫療器械注冊證過期的同類醫療器械臨床評價資料進行臨床評價嗎? 由于醫療器械注冊證是許可類證書,有5年的有效期,不少醫療器械注冊崗位小伙伴在選擇同類可比醫療器械開展臨床評價時,發現拿到的醫療器械注冊證信息已經超過有效期,并且不清楚對比企業是否已經完成延續注冊,在此情況下,可以使用醫療器械注冊證過期的同類醫療器械臨床評價資料進行臨床評價嗎?一起看正文。 時間:2024-9-8 17:46:36 瀏覽量:663

-
醫療器械注冊產品材料介導致熱性一般應如何評價? ?依據醫療器械生物學評價標準,部分與人體接觸的醫療器械需要進行材料介導致熱性評價,本文為大吉啊介紹醫療器械注冊產品材料介導致熱性的評價要求,一起看正文。 時間:2024-9-6 0:00:00 瀏覽量:677

-
第三類醫療器械臨床試驗設計范例(生物可吸收雷帕霉素洗脫冠脈支架系統) 對于第三類醫療器械注冊產品來說,多數三類醫療器械不在免于醫療器械臨床試驗目錄內,因此,多數三類器械在項目立項階段,會細致評估醫療器械臨床試驗設計、樣本量及臨床試驗費用,本文為大家帶來第三類醫療器械臨床試驗設計范例(生物可吸收雷帕霉素洗脫冠脈支架系統)。 時間:2024-8-6 20:47:51 瀏覽量:455

-
北京上海開展優化創新藥臨床試驗審評審批試點 2024年8月2日,國家藥監局發布《關于同意在北京上海開展優化創新藥臨床試驗審評審批試點的批復》,同意在北京、上海開展優化創新藥臨床試驗審評審批試點。一起看正文。 時間:2024-8-3 20:52:55 瀏覽量:454

-
醫療器械臨床試驗嚴重不良事件網絡上報的法規依據是什么? 由于醫療器械臨床試驗多數屬于驗證性、前瞻性臨床研究,臨床試驗天生帶有不確定性,因此,醫療器械臨床試驗嚴重不良事件(SAE)是或有事項,對于醫療器械臨床試驗項目管理者和執行者來說,一定要掌握醫療器械臨床試驗嚴重不良事件網絡上報及其相關要求,一起看正文。 時間:2024-8-1 21:23:50 瀏覽量:612

-
髂靜脈支架系統臨床試驗設計要點及樣本量 髂靜脈支架系統在我國屬于第三類醫療器械注冊產品,且不在豁免臨床試驗目錄之內,因此,醫療器械注冊人需要通過醫療器械臨床試驗路徑完成臨床評價,本文為大家介紹髂靜脈支架系統臨床試驗設計要點及樣本量。 時間:2024-7-30 14:08:14 瀏覽量:513

-
按照“免于進行臨床評價”路徑申報產品,增加“同品種比對”路徑的臨床評價資料是否可行? 對于醫療器械注冊項目來說,醫療器械臨床評價路徑和方式是立項前重點考量要素之一,醫療器械臨床評價路徑包括免于進行臨床評價、同品種比對臨床評價和醫療器械臨床試驗三種路徑,本文為大家帶來臨床評價答疑1項,一起看正文。 時間:2024-7-17 0:00:00 瀏覽量:451

-
持續葡萄糖監測系統在原有成人適用范圍基礎上新增兒童范圍的臨床試驗要求? 持續葡萄糖監測系統(Continuous Glucose Monitoring System,CGMS)目前批準適用范圍一般為“產品用于糖尿病成年患者(≥18歲)的組織間液葡萄糖水平的連續或定期監測。持續葡萄糖監測系統在原有成人適用范圍的基礎上新增申報兒童的適用范圍,如何進行臨床試驗?一起看正文。 時間:2024-6-25 21:57:52 瀏覽量:554

-
國家藥監局部署加強醫療器械臨床試驗機構監管 來自國家藥監局官網近日文章,醫療器械臨床試驗是證明醫療器械產品上市安全性、有效性的重要過程和保障,醫療器械臨床試驗機構在保障臨床試驗質量和保護受試者權益方面發揮著至關重要作用,國家藥監局部署加強醫療器械臨床試驗機構監管。 時間:2024-6-11 22:17:33 瀏覽量:540

-
我國判定醫療器械臨床評價路徑常用法規文件 對于醫療器械注冊項目來說,準確判定產品是否需要開展醫療器械臨床試驗,是否可以通過同品種臨床評價路徑完成臨床評價,是否屬于免于醫療器械臨床評價產品,對注冊項目決策和醫療器械注冊實施工作都極其重要,本文為大家說說我國判定醫療器械臨床評價路徑常用法規文件。 時間:2024-5-31 21:34:44 瀏覽量:516

-
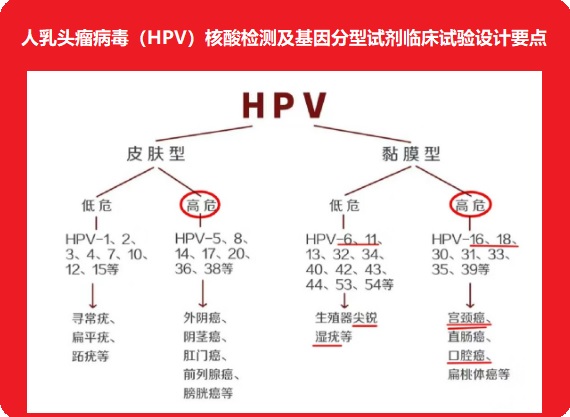
人乳頭瘤病毒(HPV)核酸檢測及基因分型試劑臨床試驗設計要點 人乳頭瘤病毒(HPV)核酸檢測及基因分型試劑是指利用包括PCR-熒光探針法或其他分子生物學方法在內的核酸檢測技術,以特定高危型HPV核酸(包括DNA和RNA)序列為檢測目的,對人宮頸脫落上皮細胞進行體外定性檢測的試劑,以確定受試樣本中是否存在高于陽性判斷值水平的高危型HPV病毒,或同時鑒定感染HPV的基因型別。 時間:2024-4-23 18:53:20 瀏覽量:691
-
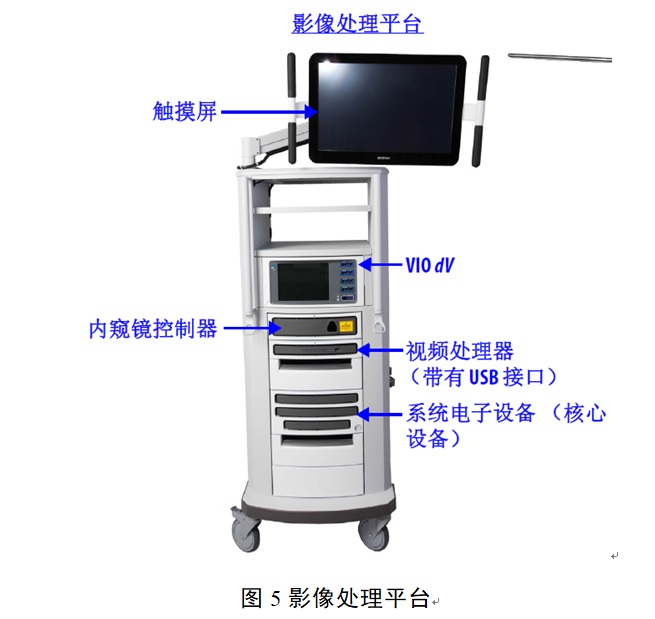
腹腔內窺鏡手術系統臨床試驗設計要點及注意事項 多孔腹腔內窺鏡手術系統(簡稱手術系統)通常包括醫生控制臺、患者手術平臺、影像處理平臺、三維腹腔內窺鏡(簡稱內窺鏡)、手術器械等。按現行《醫療器械分類目錄》,該類產品在我國屬于第三類醫療器械注冊產品,分類編碼為01-07-03。本文為大家說說腹腔內窺鏡手術系統臨床試驗設計要點及注意事項。 時間:2024-4-22 20:35:03 瀏覽量:626
-
廣東某企業因醫療器械臨床試驗真實性問題被罰 2024年4月16日,國家藥監局發布《關于醫療器械臨床試驗監督抽查情況的通告(2024年第15號)》,廣東和信健康科技有限公司申報注冊的呼吸道合胞病毒、甲型流感病毒、乙型流感病毒、腺病毒抗原聯合檢測試劑盒(流式細胞儀法-FITC/PE/Cy5/PC7)(受理號:CSZ2100014)存在臨床試驗真實性問題。一起看正文。 時間:2024-4-17 19:34:25 瀏覽量:713

