醫療器械優先審批程序
一、什么類型的產品可以申請醫療器械優先審批程序?
1.診斷或者治療罕見病、惡性腫瘤且具有明顯臨床優勢,診斷或者治療老年人特有和多發疾病且目前尚無有效診斷或者治療手段,專用于兒童且具有明顯臨床優勢,或者臨床急需且在我國尚無同品種產品獲準注冊的醫療器械;
2.列入國家科技重大專項或者國家重點研發計劃的醫療器械;
3.國家藥品監督管理局規定的其他可以適用優先注冊程序的醫療器械。
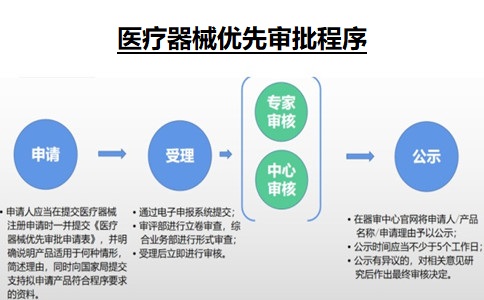
二、如何申請醫療器械優先審批程序?
申請適用優先注冊程序的,申請人應當在提出醫療器械注冊申請時,向國家藥品監督管理局提出適用優先注冊程序的申請。屬于《醫療器械注冊與備案管理辦法》第七十三條第一項情形的,由國家藥品監督管理局組織專家進行審核,符合的,納入優先注冊程序;屬于《醫療器械注冊與備案管理辦法》第七十三條第二項情形的,由國家局器械審評中心進行審核,符合的,納入優先注冊程序;屬于《醫療器械注冊與備案管理辦法》第七十三條第三項情形的,由國家藥品監督管理局廣泛聽取意見,并組織專家論證后確定是否納入優先注冊程序。
第七十五條 對納入優先注冊程序的醫療器械注冊申請,國家藥品監督管理局優先進行審評審批,省、自治區、直轄市藥品監督管理部門優先安排醫療器械注冊質量管理體系核查。
國家局器械審評中心在對納入優先注冊程序的醫療器械產品開展技術審評過程中,應當按照相關規定積極與申請人進行溝通交流,必要時,可以安排專項交流。