- 醫療器械注冊
- 第二類醫療器械注冊 第三類醫療器械注冊 進口醫療器械注冊 第一類醫療器械備案 體外診斷試劑注冊 醫療器械注冊體系考核 醫療器械生產許可證
- 醫療器械CE認證
- 醫療器械CE認證 FDA注冊(備案) 醫療器械境外注冊服務 ISO13485認證 ISO15378醫療包材體系認證 MDSAP認證服務 ISO13485內審員培訓
- 醫療器械臨床試驗
- 醫療器械臨床試驗服務 同品種比對臨床評價 體外診斷試劑(IVD)臨床試驗服務 臨床協調員(CRC)服務 進口醫療器械補充臨床試驗服務 醫院臨床試驗機構備案服務 醫療器械主文檔登記
- 醫療器械經營許可
- 醫療器械經營許可證辦理 第二類醫療器械經營備案 醫療器械網絡銷售備案 醫療器械分類界定代辦 醫療器械飛行檢查服務 醫療器械注冊檢驗資質 獸藥經營許可證辦理
- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
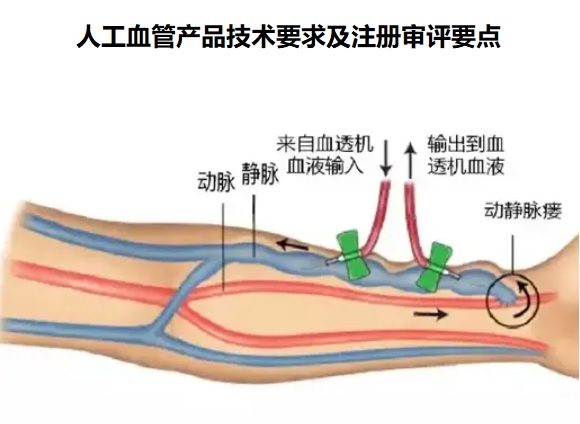
人工血管產品技術要求及注冊審評要點 適用于動靜脈瘺的建立的人工血管在我國屬于第三類醫療器械注冊產品,該產品為多層結構,在膨體聚四氟乙烯(ePTFE)內層 和聚對苯二甲酸乙二醇酯(PET)編結物外層之間,有加強型聚丙烯(PP)支撐環和硅膠層。環氧乙烷滅菌,一次性使用。本文為大家介紹人工血管產品技術要求及注冊審評要點,一起看正文。 時間:2024-12-13 23:06:48 瀏覽量:156
-
境內第三類醫療器械注冊質量管理體系核查工作程序 為做好醫療器械注冊質量管理體系核查工作,根據《醫療器械監督管理條例》(國務院令第739號)《醫療器械注冊與備案管理辦法》(國家市場監督管理總局令第47號)和《體外診斷試劑注冊與備案管理辦法》(國家市場監督管理總局令第48號)等相關規定,制定《境內第三類醫療器械注冊質量管理體系核查工作程序》。 本程序適用于境內第三類醫療器械注冊質量管理體系核查。 時間:2024-11-3 22:17:31 瀏覽量:733
-
醫療器械變更注冊申報資料清單及要求 醫療器械變更注冊流程與首次注冊基本一致,醫療器械變更注冊申報資料與首次注冊申報資料也基本上差不多,該有的都要有,但是,醫療器械變更注冊費用比首次注冊低,本文為大家醫療器械變更注冊申報資料清單及要求,一起看正文。 時間:2024-6-6 7:45:49 瀏覽量:1317

-
醫療器械延續注冊申報資料清單及要求 醫療器械延續注冊申報資料主要包括三個部分,即監管信息、非臨床資料和臨床資料,經常有客戶朋友問我醫療器械延續注冊申報資料有哪些,以及相關要求,一起看正文。 時間:2024-6-6 7:36:59 瀏覽量:1615

-
醫療器械光輻射安全注冊審查指導原則(2024年第12號) 醫療器械光輻射安全注冊審查指導原則旨在指導醫療器械注冊申請人識別產品光輻射風險并采取相應的風險控制措施,提交相應的注冊申報資料,同時指導技術審評人員對相關文件進行審評。本指導原則是對醫療器械光輻射安全的一般要求,注冊申請人需根據產品特性和風險程度確定本指導原則具體內容的適用性,若不適用詳述理由。注冊申請人亦可采用其他符合法規要求的替代方法,但需提供詳盡研究資料。 時間:2024-3-18 20:08:58 瀏覽量:1555

-
創新醫療器械申請代辦咨詢服務 擬申請醫療器械注冊的產品如果滿足創新條件,通過創新醫療器械申請將獲得許多好處,比如更好的在項目前期預見醫療器械注冊審評審批風險,更早的應對及規劃醫療器械注冊進程,當然,對于市場來說,也有諸多好處。本文為大家介紹創新醫療器械申請代辦咨詢服務。 時間:2023-12-16 21:15:20 瀏覽量:1640

-
一文讀懂醫療器械軟件 當前醫療器械行業對于醫療器械軟件存在很多認識誤區,因此有必要對常見的、關鍵的認識誤區進行解析。本文針對軟件定義、軟件風險、軟件質量與缺陷、軟件變更與版本、現成軟件的認識誤區進行了討論和分析,幫助行業從業者了解醫療器械軟件。 時間:2023-7-26 19:24:26 瀏覽量:2458

-
透明質酸鈉類面部注射填充材料臨床試驗指導原則(2019年第13號) 《透明質酸鈉類面部注射填充材料臨床試驗指導原則(2019年第13號)》雖然為該類產品的臨床試驗及注冊申請人在申請產品注冊時臨床試驗資料的準備提供了初步指導和建議,但是不會限制醫療器械相關管理部門對該類產品的技術審評、行政審批以及注冊申請人對該類產品臨床試驗資料的準備工作。本指導原則系對透明質酸鈉類面部注射填充材料臨床試驗的一般要求。 時間:2023-3-7 20:40:47 瀏覽量:2069

-
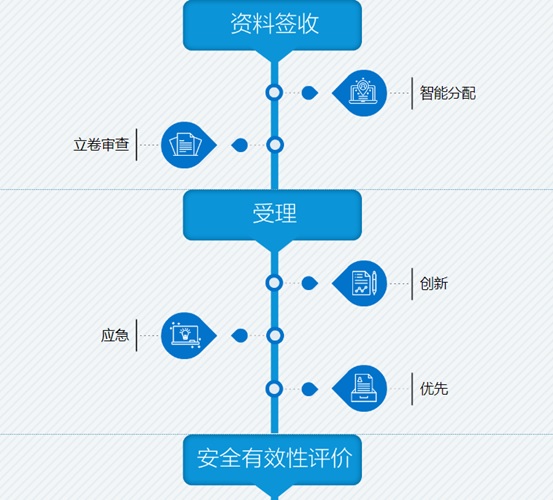
醫療器械注冊審評流程圖 醫療器械注冊審評是醫療器械注冊關鍵事項之一,了解注冊審評流程將有助于我們理解注冊審評,更好的控制醫療器械注冊項目風險。 時間:2022-6-15 20:41:38 瀏覽量:2442
-
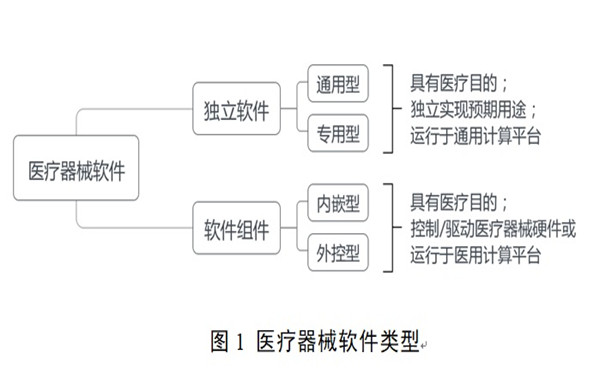
醫療器械軟件注冊審查指導原則(2022年修訂版)(2022年第9號) 為進一步規范醫療器械軟件注冊的管理,國家藥監局器審中心組織制定了醫療器械軟件注冊審查指導原則(2022年修訂版)(2022年第9號),并與2022年3月9日發布。 時間:2022-3-13 17:11:10 瀏覽量:6168
-
醫療器械網絡安全注冊審查指導原則2022年修訂版 醫療器械網絡安全注冊審查指導原則(2022年修訂版) ,旨在指導注冊申請人規范醫療器械網絡安全生存周期過程和準備醫療器械網絡安全注冊申報資料,同時規范醫療器械網絡安全的技術審評要求,為醫療器械軟件、質量管理軟件的體系核查提供參考。 時間:2022-3-9 11:09:07 瀏覽量:3875
-
人工智能醫療器械注冊審查指導原則(2022年第8號) 人工智能醫療器械注冊審查指導原則(2022年第8號),旨在指導注冊申請人建立人工智能醫療器械生存周期過程和準備人工智能醫療器械注冊申報資料,同時規范人工智能醫療器械的技術審評要求,為人工智能醫療器械、質量管理軟件的體系核查提供參考。 時間:2022-3-9 10:59:05 瀏覽量:2596

-
動物源性醫療器械注冊技術審查指導原則(2017年修訂版) 動物源性醫療器械注冊技術審查指導原則(2017年修訂版) ,本指導原則是對注冊申請人和醫療器械相關管理部門技術審評人員的指導性文件,不限制相關管理部門對該類產品的技術審評以及注冊申請人對注冊申報資料的準備工作。本指導原則不包括注冊審批所涉及的行政事項,亦不作為法規強制執行。 時間:2022-2-15 18:26:25 瀏覽量:2395

-
藥監總局醫療器械注冊審評老師聯系電話 醫療器械注冊第三方服務 時間:2022-1-12 15:30:58 瀏覽量:16752

-
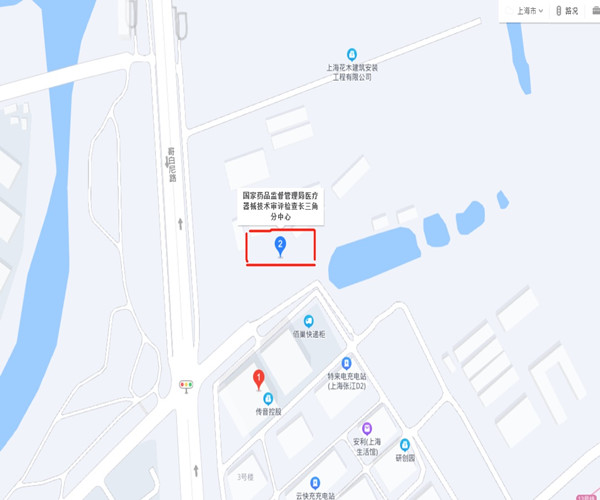
醫療器械技術審評檢查長三角分中心電話和地址 醫療器械技術審評檢查長三角分中心電話和地址 時間:2021-10-14 13:00:15 瀏覽量:3188
-
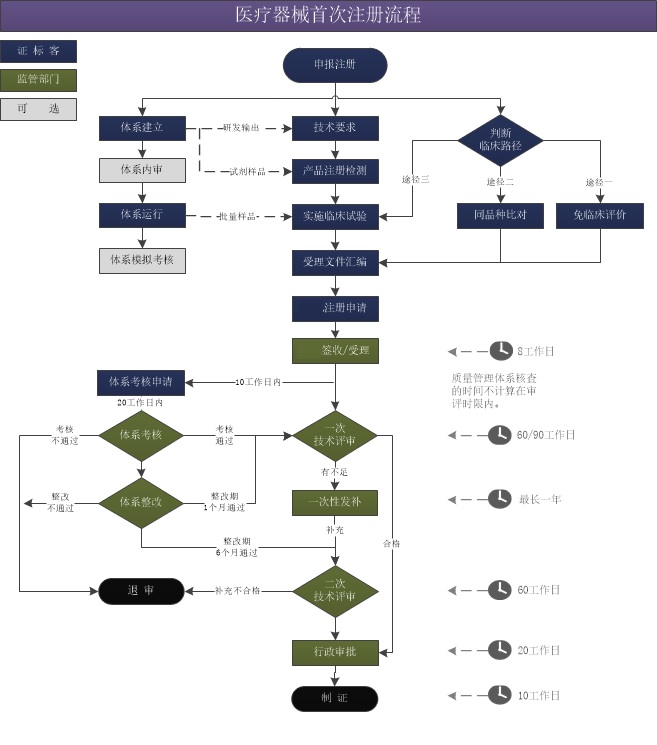
第三類醫療器械注冊流程 根據《醫療器械監督管理條例》(國務院令第650號)的規定,對醫療器械按照風險程度實行分類管理。 第Ⅰ類是風險程度低,境內生產企業需要在所在地市藥監局進行備案,境外醫療器械生產企業需要委托境內代理人在NMPA進行備案。第二類是具有中度風險,境內生產企業需要在所在地省(直轄市)藥監局進行注冊,境外醫療器械生產企業需要委托境內代理人在NMPA進行注冊。第三類類是具有較高風險,均需要在NMPA進行注冊。 時間:2021-8-16 18:41:04 瀏覽量:5175
-
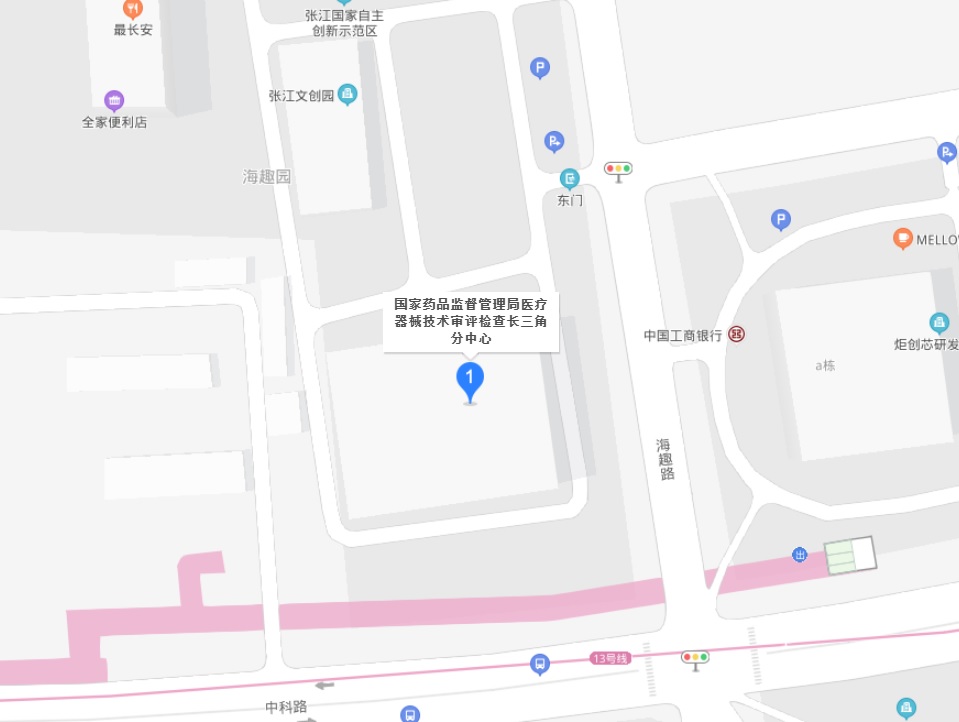
國家藥監局醫療器械技術審評檢查長三角分中心地址和電話 醫療器械技術審評檢查長三角分中心地址和電話 時間:2021-8-15 19:05:11 瀏覽量:4383
-
什么是藥械組合產品 什么是藥械組合產品,怎樣界定藥械組合產品?一起來看一下。 時間:2019-11-29 19:07:08 瀏覽量:9123

-
藥械組合產品技術審評簡介 藥械組合產品是一類特殊的醫療產品類別,一起來了解藥械組合產品技術審評。 時間:2019-11-29 19:00:15 瀏覽量:4397

