如果您之前接觸過藥包材登記事項或是藥用原輔料登記事項,那您就很容易理解醫療器械主文檔登記事項。如果您是第一次接觸醫療行業,那也沒關系,我盡力在這篇文章中把主文檔登記講通透。
如果您之前接觸過藥包材登記事項或是藥用原輔料登記事項,那您就很容易理解醫療器械主文檔登記事項。如果您是第一次接觸醫療行業,那也沒關系,我盡力在這篇文章中把主文檔登記講通透。
一、醫療器械主文檔登記的法規依據
2021年3月12日,國家藥監局發布《關于醫療器械主文檔登記事項的公告(2021年第36號)》,同日,國家藥監局發布《關于醫療器械主文檔登記事項公告》解讀。
2023年1月18日,國家藥監局發布《關于進一步明確醫療器械主文檔登記及使用有關事項的通知》,幫助我們更加準確理解相關要求。
二、醫療器械主文檔登記的對象和目的
醫療器械主文檔內容主要涉及醫療器械的原材料和某些關鍵部件,而不是成品的醫療器械。我國推動醫療器械主文檔登記的意義在于:簡化注冊流程、避免重復評審,同時有利于保證醫療器械的安全有效性。
醫療器械主文檔制度適用于醫療器械注冊申請人在我國境內提出的進口第二類、第三類及境內第三類醫療器械(含體外診斷試劑)注冊、變更、臨床試驗審批等申請事項中所引用主文檔的登記。各省、自治區、直轄市藥品監督管理局可根據實際情況參照本公告開展境內第二類醫療器械主文檔登記事項。
三、醫療器械主文檔登記流程
醫療器械主文檔登記流程如下:
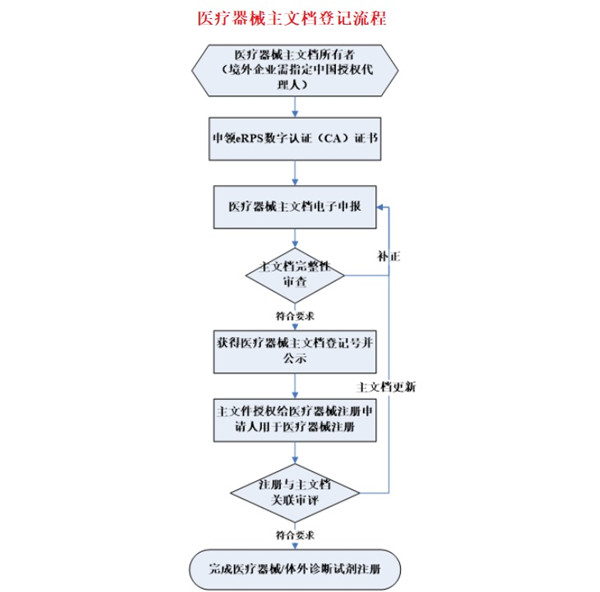
主文檔登記資料及簽章等內容適用于醫療器械注冊電子申報相關要求。主文檔所有者或其代理機構申領eRPS系統配套使用的數字認證證書(Certificate Authority,CA)后,在電子申報系統中提交醫療器械主文檔登記申請表或醫療器械主文檔登記更新申請表、申請表隨附登記資料、技術資料等登記資料。資料提交成功后,器審中心向主文檔所有者或其代理機構發送醫療器械主文檔登記回執。登記回執僅證明主文檔存檔待查,供醫療器械產品注冊等申報事項引用。國家藥監局器審中心將適時在其官方網站公開主文檔登記相關信息,以便于公眾查詢。
四、醫療器械主文檔登記資料包括哪些內容?
醫療器械主文檔是一種技術資料形式,此資料主要包括醫療器械原材料的技術資料:原材料組成成分描述、理化性能研究資料、生物學評價資料、毒理學風險分析資料等。

醫療器械主文檔所有者按照醫療器械注冊申報資料相關要求建立主文檔。醫療器械主文檔登記包括企業基本信息和產品技術資料。
醫療器械主文檔的內容可以涉及醫療器械多個方面,包括原材料等。醫療器械主文檔需要包括具體技術內容,如原材料主文檔可以包括原材料組成成分描述、物理性能研究資料、化學性能研究資料、生物學評價資料/毒理學風險分析資料等。
主文檔的技術內容建議參照醫療器械/體外診斷試劑注冊申報資料要求以及相關指導原則的適用要求提供。
五、醫療器械主文檔在哪里辦理登記?
國家藥品監督管理局醫療器械技術審評中心(以下簡稱器審中心)建立醫療器械主文檔登記平臺(以下簡稱為登記平臺)與數據庫。主文檔所有者可通過登記平臺按本公告要求提交主文檔登記資料,登記后獲得主文檔登記編號。器審中心待關聯醫療器械提出注冊相關申請后對主文檔資料一并審評。
六、如何查詢已辦理醫療器械主文檔登記信息
主文檔所有者可通過登記平臺按本公告要求提交主文檔登記資料,登記后獲得主文檔登記編號。器審中心在官方定期公式相關信息。

七、醫療器械主文檔登記是強制行為還是自愿行為?
醫療器械主文檔的登記為自愿行為。境內主文檔所有者可自行申請登記。進口(含港澳臺地區)主文檔所有者應當委托境內代理機構申請登記。主文檔登記資料均需經過主文檔所有者簽章,包括醫療器械主文檔登記(更新)申請表及其隨附登記資料和技術資料。外文文件還需提供簡體中文翻譯件(中文翻譯件可由境內代理機構簽章)。
醫療器械主文檔是技術資料的一種形式,該類資料由其所有者直接提交給醫療器械監管機構,用于授權醫療器械產品注冊申請人在申報醫療器械注冊等事項時使用。醫療器械主文檔的登記為自愿行為。
八、醫療器械主文檔資料的知識產權被如何保護?
當醫療器械申請人在申報產品注冊中需要使用主文檔資料時,主文檔所有者向醫療器械申請人出具授權書。醫療器械申請人將該授權書作為申報資料的一部分。
當監管機構對醫療器械申報資料審評時,可依據授權書調閱已登記的主文檔資料進行審評。
對醫療器械注冊申報資料的保密原則、保密措施等,均適用于主文檔資料。
九、其它要求
已登記的醫療器械主文檔內容發生變化時,主文檔所有者可申請登記資料的更新。