甘肅下轄12個地級市�、2個自治州,是西北地區(qū)經(jīng)濟(jì)和政治中心之一����,也有非常好的醫(yī)療產(chǎn)業(yè)基礎(chǔ)�����,正好因?yàn)楣ぷ鞒霾畹礁拭C武威,寫個文章為大家科普有關(guān)甘肅第二類醫(yī)療器械產(chǎn)品注冊流程?和要求�����。
甘肅下轄12個地級市����、2個自治州,是西北地區(qū)經(jīng)濟(jì)和政治中心之一,也有非常好的醫(yī)療產(chǎn)業(yè)基礎(chǔ)�,正好因?yàn)楣ぷ鞒霾畹礁拭C武威�,寫個文章為大家科普有關(guān)甘肅第二類醫(yī)療器械產(chǎn)品注冊流程和要求�。
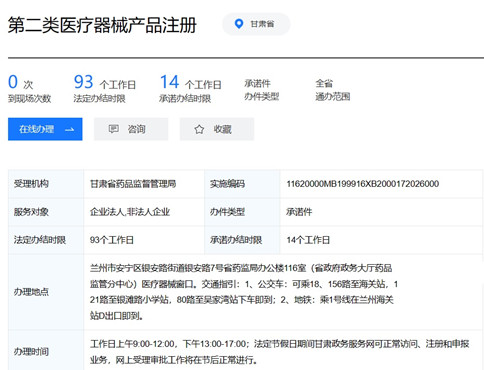
一、甘肅第二類醫(yī)療器械產(chǎn)品注冊要多少時間?
1、受理之日起�,3個工作日內(nèi)將申報資料轉(zhuǎn)交技術(shù)審評機(jī)構(gòu)�����;60個工作日內(nèi)完成第二類醫(yī)療器械注冊的技術(shù)審評工作;技術(shù)審評結(jié)束后20個工作日內(nèi)作出決定;10個工作日內(nèi)發(fā)給醫(yī)療器械注冊證。
2�����、技術(shù)審評過程中需要申請人補(bǔ)正資料的����,申請人應(yīng)當(dāng)在1年內(nèi)按照補(bǔ)正通知的要求一次提供補(bǔ)充資料;技術(shù)審評機(jī)構(gòu)應(yīng)當(dāng)自收到補(bǔ)充資料之日起60個工作日內(nèi)完成技術(shù)審評����。申請人補(bǔ)充資料的時間不計算在審評時限內(nèi)。
二����、甘肅第二類醫(yī)療器械產(chǎn)品注冊受理?xiàng)l件:
1�����、醫(yī)療器械注冊應(yīng)遵守相關(guān)法律�����、法規(guī)、規(guī)章、強(qiáng)制性標(biāo)準(zhǔn),遵循醫(yī)療器械安全和性能基本原則,參照相關(guān)技術(shù)指導(dǎo)原則����,證明注冊����、備案的醫(yī)療器械安全�����、有效�����、質(zhì)量可控,保證全過程信息真實(shí)、準(zhǔn)確、完整和可追溯。
2�、申請人����、備案人應(yīng)當(dāng)為能夠承擔(dān)相應(yīng)法律責(zé)任的企業(yè)或者研制機(jī)構(gòu)�。
3����、申請人、備案人應(yīng)當(dāng)建立與產(chǎn)品相適應(yīng)的質(zhì)量管理體系�����,并保持有效運(yùn)行�。
4、辦理醫(yī)療器械注冊�����、備案事項(xiàng)的人員應(yīng)當(dāng)具有相應(yīng)的專業(yè)知識�,熟悉醫(yī)療器械注冊、備案管理的法律�、法規(guī)����、規(guī)章和注冊管理相關(guān)規(guī)定�。
5、申請注冊�����,應(yīng)按照國家藥品監(jiān)督管理局有關(guān)注冊的要求提交相關(guān)資料�,申請人、備案人對資料的真實(shí)性負(fù)責(zé)�����。
6����、注冊資料應(yīng)當(dāng)使用中文�。根據(jù)外文資料翻譯的,應(yīng)當(dāng)同時提供原文�。引用未公開發(fā)表的文獻(xiàn)資料時�,應(yīng)當(dāng)提供資料權(quán)利人許可使用的文件����。
7、醫(yī)療器械應(yīng)當(dāng)符合適用的強(qiáng)制性標(biāo)準(zhǔn)�。產(chǎn)品結(jié)構(gòu)特征����、預(yù)期用途、使用方式等與強(qiáng)制性標(biāo)準(zhǔn)的適用范圍不一致的�����,申請人�����、備案人應(yīng)當(dāng)提出不適用強(qiáng)制性標(biāo)準(zhǔn)的說明�����,并提供相關(guān)資料。
8����、 醫(yī)療器械注冊應(yīng)遵循醫(yī)療器械分類規(guī)則和分類目錄的有關(guān)要求����。
三����、甘肅第二類醫(yī)療器械產(chǎn)品注冊流程:
第二類醫(yī)療器械產(chǎn)品注冊流程圖如下:
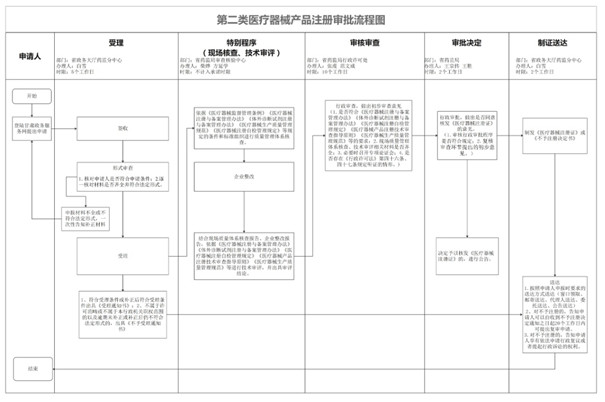
除流程圖上所示事項(xiàng)之外�����,企業(yè)還需要預(yù)算準(zhǔn)備第二類醫(yī)療器械注冊申報材料的時間�。