- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
引言:隨著中國加入ICH組織,CRC(臨床協調員)在醫療器械臨床試驗質量及合規方面,扮演著越來越重要的角色。我們看到,越來越多的研究中心、申辦方要求CRC進入醫療器械臨床試驗研究項目。我們一起來了解一下CRC在臨床試驗中的職責。
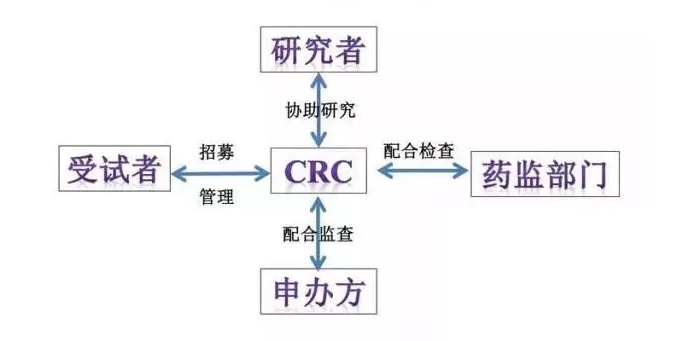
一、CRC與醫療器械臨床試驗相關方:
CRC既臨床協調員,從名稱我們也可以猜到,在醫療器械臨床試驗中的溝通協調是CRC的主要工作之一。在醫療器械臨床試驗中,CRC需要與申辦方、受試者、研究者、藥監部門、研究中心臨床研究機構等相關方密切溝通,做好協調工作。
二、CRC在醫療器械臨床試驗中的主要職責:
CRC在醫療器械臨床試驗中協助研究者進行指定臨床試驗項目中的非醫學判斷類工作,主要工作內容包括:
(1)協助研究者開展非醫學判斷相關的工作,進行受試者的篩選工作,具體包括:從病歷庫或門診病人中收集潛在受試者;對現有病人進行初步排除;檢查研究者的入排表格是否有遺漏或邏輯錯誤。定期向甲方提交受試者篩選進度相關記錄。
(2)受試者隨訪:按照醫療器械臨床試驗方案,協助研究者完成受試者隨訪工作,包括安排受試者訪視、各項檢查、獲取檢查結果并找研究者審閱簽字等。并協助研究者審閱受試者記錄是否完整等。
(3)負責或協助入組受試者的管理(原始文檔管理,包括門診和住院病歷,研究專用病歷,研究者文件的管理、CRF填寫、隨訪管理——提醒研究者醫囑并檢查執行情況),每周五下班前提交本周工作匯總給乙方GCP辦公室、研究者及甲方CRA。
(4)如遇受試者脫落或退組,CRC需協助研究者處理及記錄相關信息。提供受試者脫落或退組的相關信息郵件發送給CRA和甲方。
(5)協助研究者上報SAE:在獲知SAE發生的24小時內,CRC協助研究者填寫SAE表格后上報PI審核,確需上報,則按相關程序向有關部門報告SAE。提醒研究者對不良事件的處理、記錄及跟蹤隨訪。
(6)每周提交周報給GCP辦公室,接受GCP機構管理,有入組患者和篩選患者時或其它重要文件發生時需詳細匯報工作情況。
(7)申辦方或管理部門的稽查和視察的配合和協調。
(8)票據管理。
(9)多方溝通及記錄,協調或協助研究者完成相關病例的答疑工作。
(10)試驗物資管理等事項。
