理解和掌握全自動流式熒光免疫分析儀注冊要點及適用法規標準要求,及該類產品的工作原理、主要結構、性能指標、適用范圍等內容,將幫助醫療器械注冊?申請人應依據申報產品的具體特點,遵循相關法規的要求完成醫療器械注冊項目規劃及注冊申報資料編制。
理解和掌握全自動流式熒光免疫分析儀注冊要點及適用法規標準要求,及該類產品的工作原理、主要結構、性能指標、適用范圍等內容,將幫助醫療器械注冊申請人應依據申報產品的具體特點,遵循相關法規的要求完成醫療器械注冊項目規劃及注冊申報資料編制。
一、全自動流式熒光免疫分析儀注冊相關技術文件要求
全自動流式熒光免疫分析儀注冊相關的技術文件包括:(審
評直接相關的)法規文件、標準、指導原則等文件,本列表
不包括醫療器械行業更基礎的相關標準如質量體系、風險分
析、標簽圖示等, 也不包括有其他特殊情況下需要使用的
標準,審評人員應在了解產品的基礎上,根據產品實際情況擴展所需的技術資料。
二、全自動流式熒光免疫分析儀注冊產品的結構組成和適用范圍
產品名稱:應為通用名稱,并符合《醫療器械通用名稱命名規則》(國家食品藥品監督管理總局令第 19 號)和國
家標準、行業標準中的通用名稱要求。產品名稱由一個核心詞和不超過三個的特征詞組成。實際應用中,根據產品的結
構和性能,常采用的名稱有:全自動流式熒光免疫分析儀、流式點陣發光分析儀、流式點陣儀。
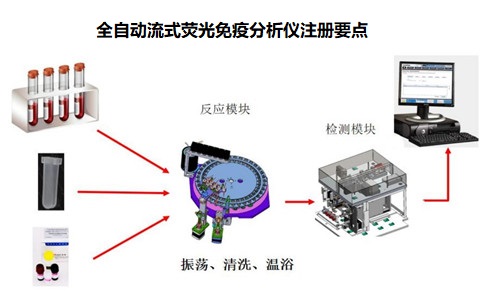
結構組成:全自動流式熒光免疫分析儀通常由主機、專用軟件組成。其中主機由加樣模塊、反應模塊、光學檢測模塊、供應模塊、廢液處理模塊組成。專用軟件可安裝在由客戶根據配置要求自行配備的計算機上,主要用于儀器的程控
操作、檢測結果的數據處理和指示判定。應當根據擬申報產品的具體特征詳細描述各組成模塊、各模塊的具體組成部分以及各主要元器件的名稱和生產企業,并詳細描述申報產品的主要功能及各組成模塊的功能,可以采用照片結合文字描述的形式給予明確說明。
產品適用范圍:預期用于與含有適用的熒光編碼微球的試劑配合使用,用于人體樣本中待測物的定性和/或定量分析。
三、全自動流式熒光免疫分析儀注冊產品分類
根據分類原則及標管中心對同類產品分類的告知,產品管理類別為第二類,分類編碼為 22-04-03。
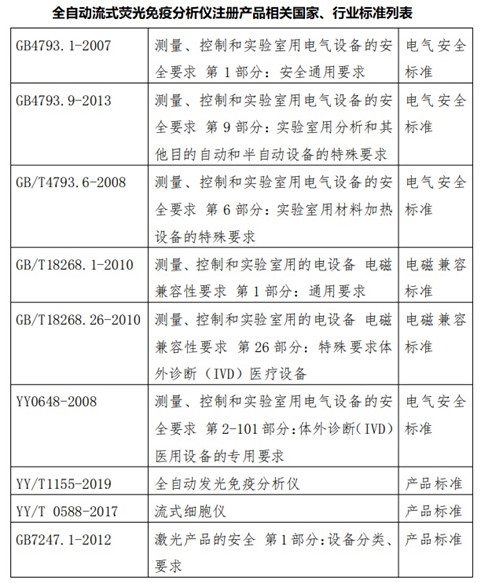
四、全自動流式熒光免疫分析儀注冊產品相關國家、行業標準列表
五、全自動流式熒光免疫分析儀注冊產品相關指導原則
1.《醫療器械軟件注冊技術審查指導原則》(2022 年修訂版)
2.《醫療器械網絡安全注冊技術審查指導原則》(2022 年修訂版)
3.《人工智能醫療器械注冊審查指導原則》
4.《全自動化學發光免疫分析儀技術審查指導原則》