安徽宣城廣德毗鄰浙江湖州長興,政府行政服務非常好,適合醫療器械產業投資、發展。昨天出差到廣德,順道為大家科普一下安徽宣城廣德第一類醫療器械產品備案流程和要求。

一、第一類醫療器械產品備案受理條件:
申報備案的產品為已列入第一類醫療器械產品目錄的醫療器械及體外診斷試劑分類子目錄中的第一類體外診斷試劑,或經分類界定屬于第一類醫療器械產品。對于第一類醫療器械產品目錄中未包含的產品,可按照《醫療器械監督管理條例》(國務院令第650號)第十六條的規定執行。
二、第一類醫療器械產品備案資料清單:
1. 第一類醫療器械備案表
2. 安全風險分析報告
3. 產品技術要求
4. 產品檢驗報告
5. 臨床評價資料
6. 產品說明書及最小銷售單元標簽設計樣稿
7. 生產制造信息
8. 企業營業執照
9. 符合性聲明
三、第一類醫療器械產品備案流程:
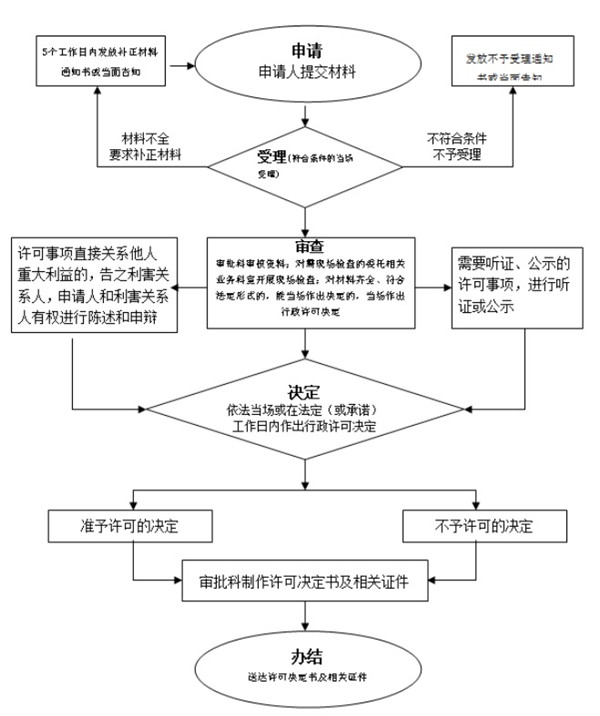
任何疑問,歡迎您隨時方便與杭州證標客醫藥技術咨詢有限公司葉工聯系,電話:18058734169,微信同。